テクノロジー・材料
メタノールを効率よくエネルギー変換する酵素の立体構造を解明
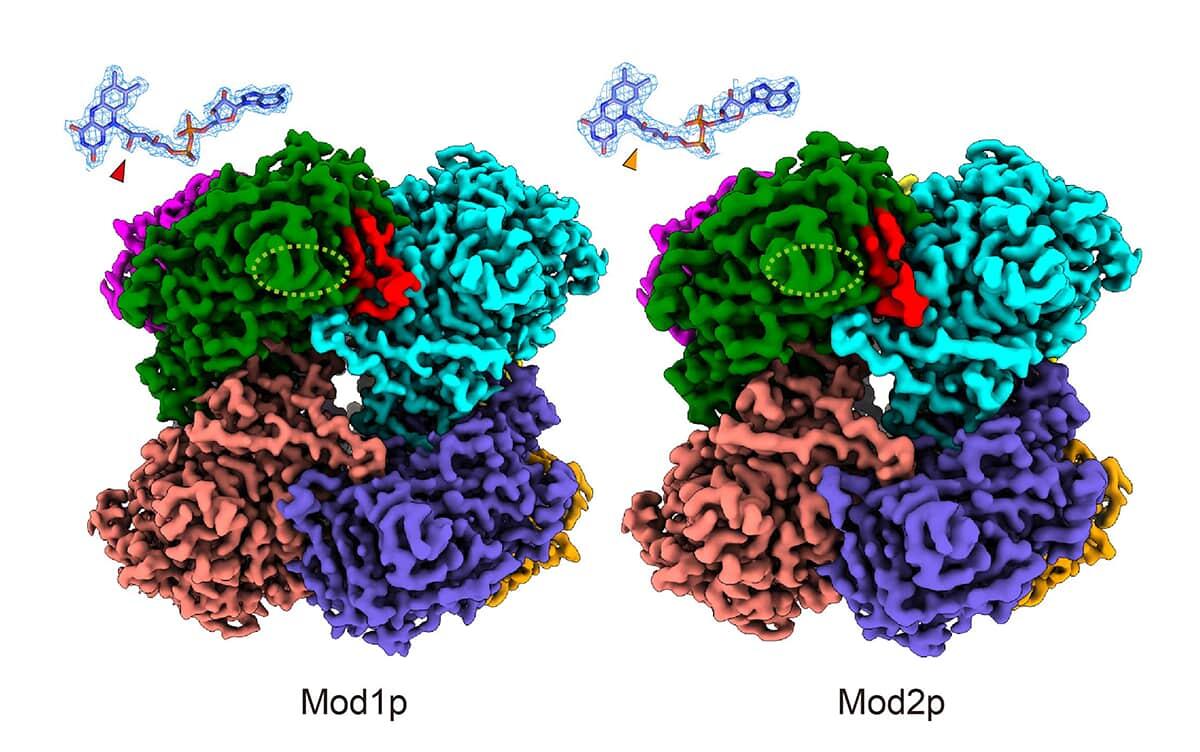
メタノールをエネルギー源として利用する酵母において重要な役割を担う酵素の立体構造を、クライオ電子顕微鏡を用いて高精度で解明しました。その結果、よく似た構造の2種類の酵素が環境に応じて異なる働きをする仕組みが明らかとなりました。
カーボンニュートラル社会の実現に向けて、メタノールの効率的な資源化が注目されています。本研究では、より効率的なメタノール利用の鍵を探るため、メタノールで成長する酵母 Ogataea methanolica におけるアルコールオキシダーゼ(AOD)という酵素に着目し、その構造と機能の違いをクライオ電子顕微鏡を用いて明らかにしました。AODには複数の種類があり、細胞のエネルギー代謝の出発点となる、メタノールをホルムアルデヒドへと変換する反応においては、それぞれ異なる働きをすることで円滑なメタノール代謝を実現していることが知られていましたが、そのような性質の違いが生じる理由はこれまで明らかではありませんでした。
本研究では、各AODの立体構造を詳細に比較しました。その結果、全体の構造は類似しているものの、酵素の働きを助ける補酵素の結合様式や、周囲のアミノ酸配置に違いがあることが分かりました。これらの違いが酵素の安定性や電子伝達効率に影響し、結果として酵素活性の差異を生み出している可能性が示唆されました。さらに、タンパク質外周の構造の違いが、酵素活性の安定化に関与していることも明らかになりました。これらの知見から、わずかな構造差が酵素機能に大きな影響を与えることが示されました。この成果は、酵素の分子機構の理解を深めるとともに、高効率な酵素設計や、微生物や酵素を利用したバイオプロセス開発につながると期待されます。
PDF資料
プレスリリース研究代表者
筑波大学計算科学研究センター谷 一寿 教授
岐阜大学応用生物科学部
中川 智行 教授
理化学研究所放射光科学研究センター/東北大学多元物質科学研究所
米倉 功治 グループディレクター/教授
掲載論文
- 【題名】
-
Cryo-EM structures of alcohol oxidase isozymes reveal structural determinants of cofactor variation and enzymatic activity in Ogataea methanolica
(Ogataea methanolica由来アルコールオキシダーゼのクライオ電子顕微鏡構造による補酵素の多様性および酵素活性決定機構の解明) - 【掲載誌】
- Microbial Biotechnology
- 【DOI】
- 10.1111/1751-7915.70355


